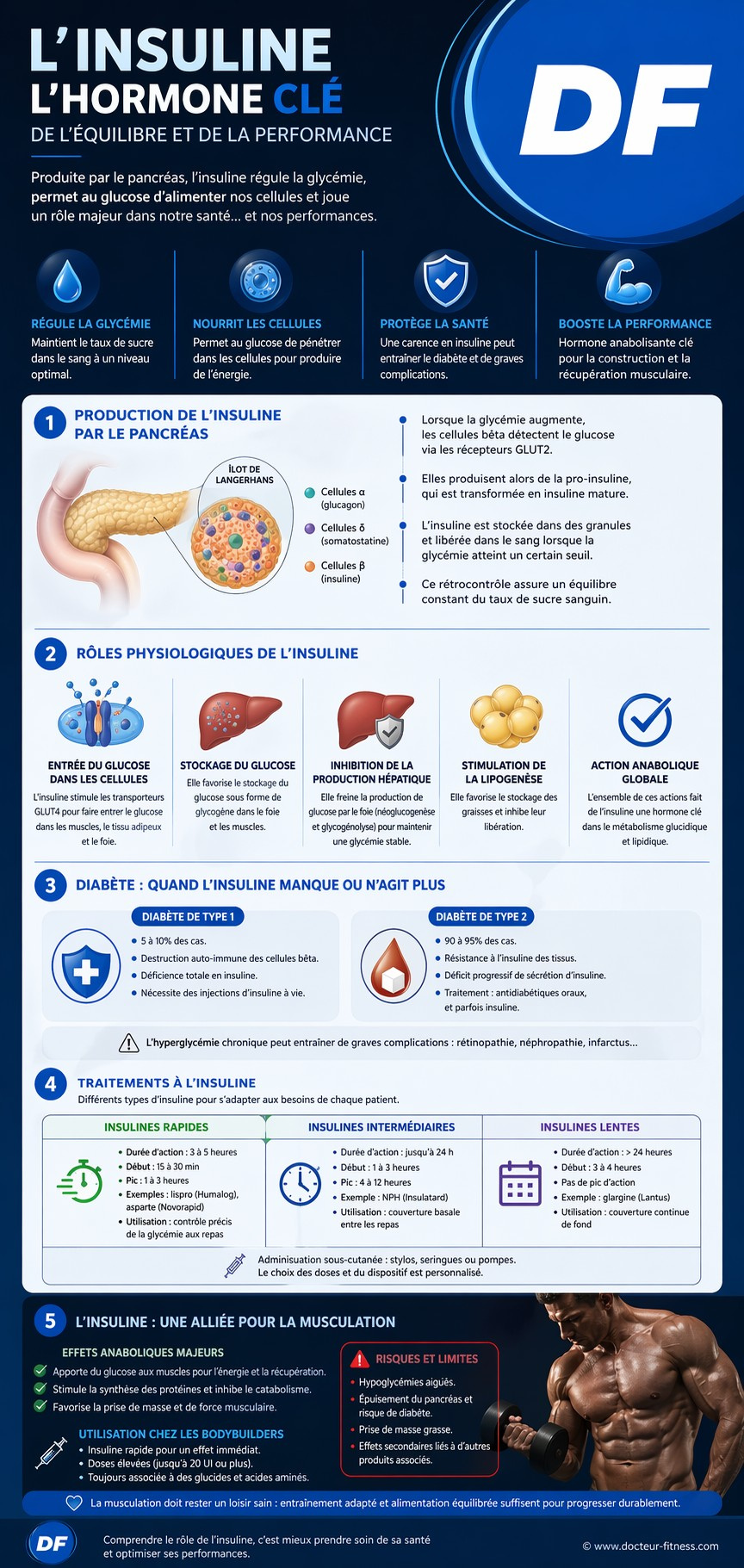
L’insuline est une hormone essentielle à la régulation des taux de sucre dans le sang, également appelée glycémie. Produite par le pancréas, l’insuline permet au glucose sanguin de pénétrer dans les cellules de l’organisme et d’être utilisé comme source d’énergie. Sans insuline, le glucose s’accumule dans le sang et provoque à terme un diabète. Comprendre le rôle de cette hormone est donc primordial pour prévenir et traiter cette maladie.

Table des matières
Production d’insuline par le pancréas
Le pancréas est une glande située derrière l’estomac, en forme de V. Il est constitué de cellules exocrines qui sécrètent des enzymes digestives, et de cellules endocrines groupées en amas appelés îlots de Langerhans.
Ces îlots pancréatiques renferment plusieurs types de cellules. Les cellules alpha sécrètent du glucagon, les cellules delta de la somatostatine, et les cellules bêta de l’insuline. Ce sont donc les cellules bêta qui sont responsables de la production d’insuline.
Lorsque le taux de glucose dans le sang augmente après un repas par exemple, les cellules bêta détectent cette augmentation grâce à des récepteurs GLUT2 situés sur leur membrane. En réponse, elles activent la transcription du gène de l’insuline et la traduction de l’ARN messager en pro-insuline.
Cette pro-insuline est clivée pour donner de l’insuline mature qui est stockée dans des granules de sécrétion. Lorsque la glycémie atteint un certain seuil, ces granules fusionnent avec la membrane cellulaire et libèrent l’insuline dans la circulation sanguine.
Il existe donc un rétrocontrôle permanent du taux de glucose sanguin sur la sécrétion d’insuline par les cellules bêta pancréatiques.
Rôles physiologiques de l’insuline
Une fois sécrétée dans le sang, l’insuline agit sur de nombreux tissus cibles possédant à leur surface des récepteurs à l’insuline : muscles, tissu adipeux, foie… Son action permet :
- L’entrée du glucose sanguin dans les cellules : l’insuline stimule la translocation à la membrane plasmique des transporteurs GLUT4 permettant au glucose de pénétrer à l’intérieur des cellules. Cet effet se manifeste dans les muscles, le tissu adipeux et le foie.
- Le stockage du glucose sous forme de glycogène hépatique et musculaire : l’insuline active la glycogène synthase, enzyme permettant la polymérisation du glucose en glycogène. Ce mécanisme constitue une réserve énergétique mobilisable en cas de besoin.
- L’inhibition de la néoglucogenèse et de la glycogénolyse hépatique : la production endogène de glucose par le foie est freinée en présence d’insuline, permettant de réguler précisément la glycémie.
- La stimulation de la lipogenèse : l’insuline induit la conversion du glucose en acides gras et en triglycérides, stockés dans le tissu adipeux. Elle inhibe également la lipolyse, empêchant la libération des acides gras.
L’ensemble de ces actions anaboliques fait de l’insuline une hormone clé dans le contrôle du métabolisme glucidique et lipidique.
Diabète et déficience en insuline
Le diabète de type 1
Il représente 5 à 10% des cas de diabète. Il est causé par la destruction auto-immune des cellules bêta pancréatiques produisant l’insuline. Ce processus inflammatoire fait intervenir les lymphocytes T, provoquant à terme une carence insulinique totale.
Sans insuline, le glucose ne peut plus pénétrer dans les cellules et s’accumule dans le sang. Malgré la production de corps cétoniques, carburant de substitution, un coma acidocétonique mortel peut survenir.
Le traitement repose sur des injections d’insuline tout au long de la vie du patient.
Le diabète de type 2
C’est la forme la plus fréquente puisqu’elle concerne 90 à 95% des diabétiques. Elle résulte le plus souvent de facteurs environnementaux et génétiques conduisant à deux anomalies :
- Une résistance à l’insuline des tissus cibles : les récepteurs sont moins sensibles à l’action de l’insuline ou en nombre insuffisant. Pour compenser, le pancréas augmente sa sécrétion d’insuline, entretenant cette résistance.
- Un déficit progressif de la sécrétion d’insuline, les cellules bêta s’épuisant à produire en excès cette hormone.
L’hyperglycémie chronique entraîne à terme des complications micro et macro-vasculaires (rétinopathie, néphropathie, infarctus…). Le traitement repose sur des antidiabétiques oraux, et parfois l’insulinothérapie.
Traitements à l’insuline
Le traitement par insuline vise à remplacer l’insuline naturelle qui fait défaut chez les personnes atteintes de diabète de type 1 et à surmonter la résistance à l’insuline des cellules chez les diabétiques de type 2. Différents types d’insuline médicamenteuse sont disponibles pour reproduire au mieux la sécrétion physiologique :
Les insulines rapides
- Durée d’action courte (3 à 5 heures) ;
- Début d’action : 15 à 30 minutes après l’injection ;
- Pic d’action : 1 à 3 heures après l’injection ;
- Exemples : insuline lispro (Humalog), insuline asparte (Novorapid) ;
- Utilisation : contrôle précis de la glycémie aux repas.
Les insulines intermédiaires
- Durée d’action moyenne (jusqu’à 24 heures) ;
- Début d’action : 1 à 3 heures ;
- Pic d’action : 4 à 12 heures ;
- Exemple : insuline NPH (Insulatard) ;
- Utilisation : couverture basale entre les repas.
Les insulines lentes
- Durée d’action longue (> 24 heures) ;
- Début d’action : plus lent (3 à 4 heures) ;
- Pas de pic d’action ;
- Exemple : insuline glargine (Lantus) ;
- Utilisation : couverture continue de fond.
Ces insulines s’injectent par voie sous-cutanée à l’aide de stylos, seringues ou pompes. Le choix du dispositif et des doses se fait sur mesure pour chaque patient selon son profil.
L’insuline : une hormone clé pour la musculation
L’insuline est une hormone anabolisante, c’est-à-dire qu’elle stimule la construction musculaire. En effet, elle exerce de puissants effets :
- Transport du glucose vers les cellules musculaires, fournissant ainsi un carburant pour la contraction et la récupération ;
- Augmentation de la synthèse protéique et inhibition du catabolisme, permettant une fixation optimale des acides aminés sous forme de nouvelles protéines musculaires ;
- Diminution de la dégradation des protéines déjà présentes dans le muscle.
L’insuline crée donc un environnement très favorable à l’augmentation de la masse et de la force musculaire. Elle agit en synergie avec d’autres hormones anaboliques comme la testostérone et l’hormone de croissance.
Protocoles d’utilisation chez les bodybuilders
Afin de maximiser ses effets, certains bodybuilders utilisent des injections exogènes d’insuline :
- Généralement de l’insuline rapide pour un effet immédiat et intense ;
- Des doses élevées, jusqu’à 20 UI voire plus ;
- En association systématique avec une absorption de glucides et d’acides aminés pour éviter l’hypoglycémie.
De tels protocoles permettent des gains de masse musculaire très importants en peu de temps, à condition de s’entraîner intensivement et de fournir suffisamment de substrats énergétiques et plastiques aux muscles.
Risques et limites
Cependant, de telles doses supra-physiologiques comportent des dangers significatifs :
- Hypoglycémies aiguës pouvant entraîner malaises et pertes de connaissance ;
- Épuisement du pancréas à long terme avec risque de diabète ;
- Prise de masse grasse en même temps que la masse musculaire ;
- Effets secondaires des autres produits associés (stéroïdes…).
La musculation doit rester un loisir sain. Mieux vaut éviter de mettre sa vie en péril pour gagner quelques kilos de muscle ! Des programmes d’entraînement adaptés et une alimentation équilibrée suffisent pour progresser.
Résumé en image