Les glucides (autrefois appelés hydrates de carbone) sont des macromolécules composées de carbone, d’hydrogène et d’oxygène. Les glucides sont utilisés par l’organisme principalement pour produire rapidement de l’énergie. Les deux principaux types de glucides sont les glucides simples, qui ont une structure composée d’un ou de deux sucres, et les glucides complexes, qui ont une structure composée de plusieurs sucres liés ensemble. Tous les glucides ont certaines propriétés en commun, notamment :
- Les glucides simples ont une structure en anneau ;
- Les glucides complexes ont une structure linéaire ou ramifiée ;
- Les glucides sont créés par la réaction de déshydratation de sucres simples ;
- Les noms des glucides simples se terminent en “-ose” ;
- Les glucides sont utilisés pour fournir de l’énergie dans les organismes vivants.

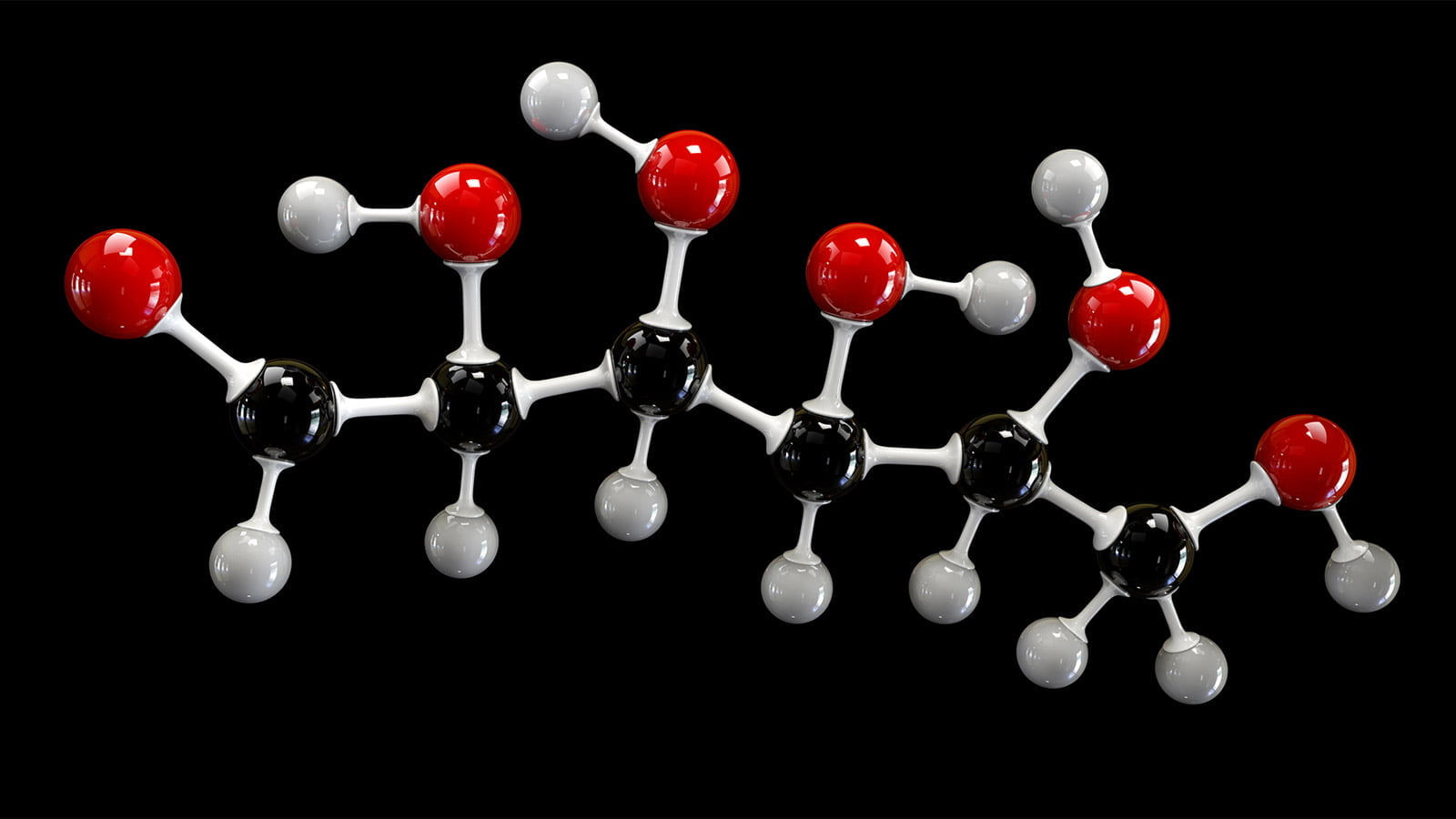
Exemples de glucides
Il existe de nombreux exemples de glucides. Voici quelques exemples biologiquement importants
- Glucose ;
- Fructose ;
- Saccharose ;
- Lactose ;
- Amidon ;
- Cellulose ;
- Glycogène.

Crédit photo © Adobe Stock
Les glucides constituent une part importante du régime alimentaire humain. Voici les sources les plus courantes de glucides :
- Pâtes ;
- Céréales ;
- Fruits ;
- Légumes ;
- Légumineuses.

Crédit photo © Adobe Stock
Caractéristiques des glucides
Compositions
Les glucides sont constitués des éléments suivants : carbone, hydrogène et oxygène. Chaque atome de carbone est lié à au moins un atome d’oxygène. Tous les glucides comprennent un groupe aldéhyde ou cétone et un groupe hydroxyle. Les glucides peuvent former de longues chaînes, qui sont soit linéaires, soit ramifiées. Mais, quelle que soit leur structure finale, tous les glucides complexes sont composés d’unités individuelles appelées monosaccharides, ou sucres simples. Chaque monosaccharide est constitué de la formule des glucides : CH2On où n est un nombre supérieur à deux.
Propriétés physiques
Les glucides constituent une classe variée de macromolécules et ont donc des propriétés physiques différentes. Le glucose, par exemple, est une poudre blanche cristalline à température ambiante. Il a un point de fusion de 153 à 156 degrés Celsius. L’amidon est un glucide complexe et contient de nombreuses molécules de glucose liées les unes aux autres. En raison de cette complexité plus importante, il a un point de fusion plus haut situé entre 256 et 258 degrés Celsius. À température ambiante, l’amidon est également une poudre cristalline blanche.
Types
Les glucides peuvent être classés en fonction du nombre de sucres présents dans la molécule. Le tableau ci-dessous résume les 3 types de glucides et donne des exemples.
| Type de glucide | Nombre de sucres | Exemples |
|---|---|---|
| Monosaccharide | Un sucre | Glucose, fructose |
| Disaccharide | Deux sucres | Lactose, saccharose |
| Polysaccharide | Trois sucres ou plus | Amidon, cellulose |
Liaison
Les monosaccharides sont reliés par des liaisons glycosidiques. Ce type de liaison n’existe que dans les glucides et relie deux monosaccharides entre eux avec un groupe éther. Les liaisons glycosidiques sont classées en fonction des éléments impliqués dans la liaison avec le carbone. La plupart des liaisons glycosidiques utilisent uniquement du carbone, de l’hydrogène et de l’oxygène, mais certaines peuvent utiliser du soufre ou de l’azote. Par exemple, une liaison N-glycosidique est un carbone attaché à un azote et est courante dans le cas de l’ajout de glucides aux protéines.
Les liaisons glycosidiques sont établies par une réaction de déshydratation, également connue sous le nom de réaction de condensation. Au cours de cette réaction, le groupe hydroxyle associé à un atome de carbone part avec un atome d’hydrogène provenant de l’autre groupe, créant ainsi de l’eau. Il existe deux principaux types de liaisons glycosidiques, la liaison 1,4-glycosidique et la liaison 1,6-glycosidique. Ces deux types de liaisons sont basés sur les atomes de carbone attachés dans les monosaccharides. C’est à partir de ces deux types de liaisons glycosidiques que la structure de la chaîne glucidique est déterminée. Une liaison 1,4-glycosidique crée une structure linéaire et la liaison 1,6-glycosidique crée une structure ramifiée.
Il existe également deux types de liaisons, alpha et bêta, qui dépendent de la stéréochimie de la liaison. Si la liaison est formée en dessous de la chaîne du glucose, la liaison est alpha et si la liaison est formée au-dessus de la chaîne, la liaison est bêta. Cela a des implications importantes pour l’homme, car le tube digestif n’est capable de décomposer que les liaisons alpha. Ainsi, les glucides d’origine végétale comme la cellulose qui utilisent des liaisons bêta ne peuvent pas être décomposés et absorbés.
Solubilité
Cette composition chimique confère aux glucides leurs propriétés physiques. Les glucides sont généralement solubles dans l’eau en raison de la polarité des liaisons entre l’oxygène et les autres atomes de la molécule. Cette polarité permet la liaison hydrogène entre les glucides et l’eau.
Ces propriétés permettent aux glucides d’être une source de carburant pour les êtres vivants en étant oxydés pendant la respiration cellulaire.
Fonctions des glucides
La principale fonction des glucides est de fournir une énergie rapide à l’organisme, mais ils ont également d’autres fonctions secondaires.
Énergie rapide
Les glucides sont utilisés comme source d’énergie rapide par les êtres vivants. Le glucose est la principale source de carburant pour la respiration cellulaire et c’est la source de carburant qui peut être utilisable le plus rapidement. Au cours de la respiration cellulaire, les cellules utilisent l’oxygène et le glucose pour produire de l’ATP, ou énergie, et le dioxyde de carbone et l’eau comme déchets. Les glucides plus volumineux comme le glycogène et l’amidon sont décomposés en sucres simples pour être utilisés dans la respiration cellulaire.
Stockage de l’énergie
Les glucides peuvent également servir à stocker de l’énergie pour les périodes où les sucres simples manquent. Chez les animaux, les glucides sont stockés sous forme de glycogène. Chez les plantes, les glucides sont stockés sous forme d’amidon, qui est composé de deux sucres complexes, l’amylopectine et l’amylose. Les humains peuvent consommer plusieurs de ces végétaux comme nourriture, comme les pommes de terre, les pois ou le maïs.
Régulation du métabolisme
La disponibilité des glucides régule également le métabolisme d’autres macromolécules comme les protéines et les lipides. Les glucides sont la source de carburant préférée de l’organisme et sont donc privilégiés par rapport aux autres macromolécules. Cela empêche les protéines structurelles importantes d’être dégradées pour servir de carburant.
Signalisation cellulaire
Les glucides sont également utilisés dans la signalisation cellulaire. De nombreuses cellules animales possèdent des glucides extracellulaires qui sont attachés aux lipides ou aux protéines de la membrane par des liaisons glycosidiques. Ces glucides de surface contribuent à la reconnaissance cellulaire et aident la cellule à identifier l’hôte par rapport aux cellules étrangères.
Structure
Les glucides sont également importants sur le plan structurel. Chez les plantes, la cellulose est un composant important de la paroi cellulaire et contribue à fournir une structure rigide et un support à la plante. La chitine est un type de glucide utilisé dans les parois cellulaires des champignons et dans l’exosquelette des arthropodes et de certains animaux marins. Chez les animaux, les glucides constituent une partie importante de la matrice extracellulaire, qui aide à ancrer les cellules en place et à fournir une charpente aux tissus.
Utilisations des glucides
Les glucides sont principalement utilisés par les êtres vivants pour fournir de l’énergie. Cependant, le corps humain a également besoin des glucides pour d’autres usages. Les fibres, comme la cellulose, sont particulièrement importantes pour la digestion. Elles aident les aliments à progresser dans le système digestif et évitent la constipation. Dans l’industrie, la cellulose est utilisée pour fabriquer de la pâte à papier et du papier. Le glucose peut également être utilisé comme matière première pour la fermentation et dans l’industrie de la production chimique.