Des centaines de milliers de personnes vivent avec un lupus. Certaines voient leurs reins lâcher sans qu’on comprenne pourquoi. Les médecins savent qu’il existe un terrain génétique, ils savent que le système immunitaire s’attaque aux propres tissus du corps. Mais le déclencheur, l’étincelle, restait une énigme.
Jusqu’à cette étude publiée dans Annals of the Rheumatic Diseases(1).
Une équipe de NYU Langone Health vient d’identifier un coupable qu’on n’attendait pas : une bactérie. Pas un virus venu de l’extérieur, pas une nouvelle molécule toxique de l’environnement. Une bactérie déjà présente dans nos intestins, y compris ceux des personnes en parfaite santé.

Table des matières
Le lupus rénal en quelques mots
Le lupus est une maladie auto-immune. Pour faire simple : le système immunitaire, qui est censé défendre le corps contre les microbes, se trompe de cible et attaque les cellules saines. Quand cette attaque se concentre sur les reins, on parle de néphrite lupique (ou lupus rénal, ou lupus néphrétique selon les médecins).
C’est la forme la plus grave de la maladie.
Les chiffres donnent le vertige. Aux États-Unis, le nombre de personnes atteintes a plus que doublé en quarante ans. Un patient sur cinq finit en insuffisance rénale terminale, la dialyse ou la greffe devenant alors la seule issue. Les femmes sont nettement plus touchées que les hommes. Les populations afro-américaines, hispaniques et asio-américaines le sont davantage que les populations caucasiennes.
Et jusqu’ici, le traitement principal consistait à éteindre le feu avec des médicaments qui musellent tout le système immunitaire. Efficaces pour certains. Inefficaces pour beaucoup. Avec des effets secondaires lourds :
- Prise de poids importante ;
- État dépressif ;
- Risque d’infection fortement majoré.
Autrement dit : on soigne sans savoir ce qu’on soigne vraiment. Et cette situation dure depuis des décennies.
Une piste qui couvait depuis plusieurs années
L’équipe du Dr Gregg Silverman, de la NYU Grossman School of Medicine, travaille depuis longtemps sur une intuition. Et si le microbiote intestinal, cet écosystème de milliards de bactéries qui vit dans nos intestins, jouait un rôle dans les poussées du lupus ?
Les premiers indices datent de plusieurs années. Des déséquilibres bactériens, que les scientifiques appellent “dysbiose”, semblaient coïncider avec les crises chez certains patients. Le nom d’une bactérie revenait souvent : Ruminococcus gnavus.
Elle est partout. Elle vit paisiblement dans les intestins de nombreuses personnes en bonne santé. En temps normal, elle ne fait ni chaud ni froid.
Mais parfois, elle prolifère. Sa population explose soudainement.
Et c’est là que tout bascule.
Ce que l’étude a trouvé chez les patientes
Les chercheurs ont analysé le sang et les selles d’un petit groupe de patientes atteintes de néphrite lupique. Chez la moitié d’entre elles, ils ont identifié une prolifération de Ruminococcus gnavus.
Toutes ces patientes partageaient deux choses : des marqueurs d’inflammation dans le sang et la présence d’anticorps dirigés contre une molécule précise. Cette molécule, c’est le cœur de la découverte.
Le lipoglycane, la pièce manquante du puzzle
La bactérie possède dans sa paroi externe une substance appelée lipoglycane. Un terme technique qui désigne une combinaison de sucres et de graisses qui tapisse la surface de certains micro-organismes.
Quand R. gnavus se multiplie de manière excessive, elle relâche ce lipoglycane en quantités anormales.
Et le système immunitaire réagit.
Il active une protéine à la surface des cellules immunitaires : le récepteur TLR2 (toll-like receptor 2). On peut se représenter ce récepteur comme une sonnette d’alarme biologique qui déclenche une réaction inflammatoire.
Sauf qu’ici, la sonnette reste coincée sur “marche forcée”.
Résultat : les plaquettes s’activent en cascade (les plaquettes sont les petites cellules du sang qui servent normalement à former les caillots), les neutrophiles (un type de globules blancs) relâchent des filets microscopiques appelés NETs, et des cellules immunitaires se mettent à produire des dégâts en série. Le profil sanguin des patientes concernées ressemble, selon les auteurs, à celui observé lors d’un sepsis : autrement dit, une infection généralisée.
Et ces dégâts finissent par atteindre les reins.
La preuve apportée par la souris
Pour vérifier que la bactérie n’était pas simplement présente par hasard, les chercheurs sont passés à l’expérience.
Ils ont colonisé l’intestin de souris sujettes au lupus avec des souches de R. gnavus productrices de lipoglycane. Les résultats parlent d’eux-mêmes :
- Activation des plaquettes observée dans le sang ;
- Infiltration des reins par des neutrophiles et des monocytes ;
- Lésions rénales proches de celles des patientes humaines ;
- Réduction nette de l’inflammation lorsque TLR2 était bloqué chez ces mêmes souris.
C’est cette dernière donnée qui change potentiellement la prise en charge future.
Un futur traitement qui ne détruirait pas tout le système immunitaire
Si le lipoglycane et TLR2 sont vraiment les déclencheurs, il devient possible d’imaginer des traitements ciblés. Plus besoin d’étouffer le système immunitaire entier : il suffirait de neutraliser la bactérie responsable ou de couper le signal d’alarme qu’elle envoie.
Plusieurs pistes sont évoquées par l’équipe de NYU Langone :
- Un antibiotique sélectif qui viserait uniquement R. gnavus, sans détruire le reste du microbiote ;
- Des anticorps anti-lipoglycane pour neutraliser la molécule à la source ;
- Des bloqueurs chimiques du récepteur TLR2 pour désactiver la réaction inflammatoire.
Des essais cliniques sont déjà envisagés.
Un test sanguin pour prédire la maladie
L’autre avancée de taille est diagnostique. La présence d’anticorps anti-lipoglycane dans le sang pourrait servir de signal précoce.
“Notre étude apporte la preuve fondatrice que la détection d’anticorps anti-lipoglycane issus de proliférations de Ruminococcus gnavus dans l’intestin pourrait identifier les personnes à risque accru de néphrite lupique”, explique le Dr Silverman, co-auteur de l’étude et titulaire de la chaire Mamdouha S. Bobst de médecine interne à la NYU Grossman School of Medicine.
Le Dr Silverman estime, dans une communication récente, que 20 à 40 % des néphrites lupiques actives observées dans les cohortes américaines pourraient correspondre à cette forme induite par le microbiote. Autrement dit : un patient sur trois à un patient sur cinq pourrait potentiellement bénéficier d’une approche totalement différente de celle utilisée aujourd’hui.
Et cela sans prendre de corticoïdes, sans immunosuppresseur lourd, sans les effets secondaires qui vont avec.
Ce qu’il faut retenir
La découverte ne signifie pas que toute personne hébergeant R. gnavus est en danger. La bactérie existe chez des individus en parfaite santé, à faibles niveaux, sans déclencher aucune réponse immunitaire. Le problème vient des proliférations soudaines, qui semblent coïncider avec les poussées de la maladie.
Les auteurs l’écrivent clairement : il faudra confirmer ces résultats sur des cohortes plus larges avant d’envisager un changement réel en clinique. Le groupe étudié reste petit. Les mécanismes pour d’autres populations (hommes, groupes ethniques différents) demandent à être vérifiés.
Mais pour la première fois, une étude relie de manière causale une bactérie intestinale, une molécule précise, un récepteur immunitaire identifié et les dégâts rénaux du lupus. Cela ouvre une porte longtemps fermée : celle d’un traitement qui s’attaquerait à la cause plutôt qu’aux symptômes.
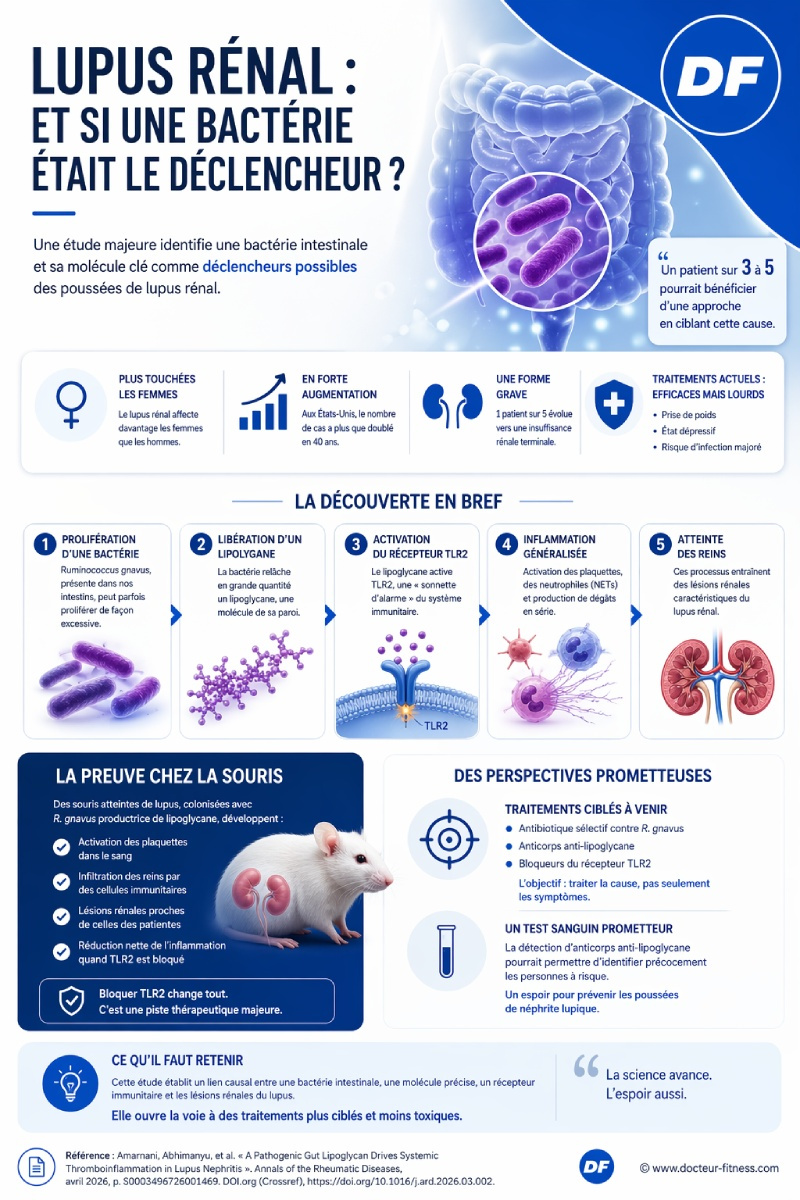
Résumé en image
Sur le même sujet
Sources éditoriales et fact-checking