Pendant des décennies, la maladie d’Alzheimer a été présentée comme une fatalité du grand âge. Une roulette génétique. Un mauvais tirage que personne ne voit venir, jusqu’au jour où les clés disparaissent, puis les prénoms, puis les visages.
Et si tout cela était faux ?
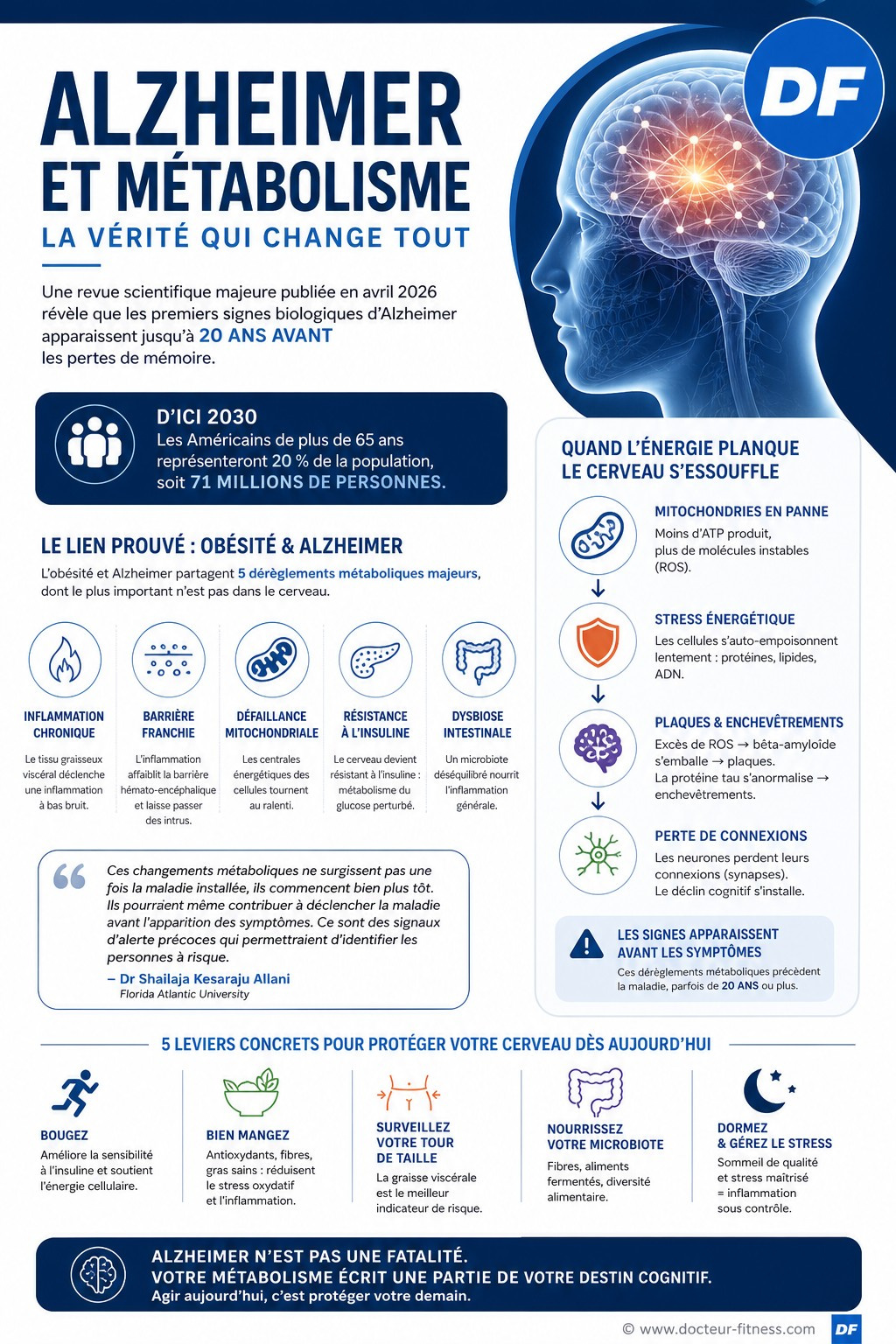
Une revue scientifique publiée dans la revue Cells(1) vient de bousculer cette image. Elle réunit des centaines d’études et arrive à une conclusion qui dérange : les premiers signes biologiques d’Alzheimer apparaîtraient bien avant les pertes de mémoire. Parfois 20 ans avant. Et ces signes ne se cachent pas dans le cerveau. Ils se cachent ailleurs dans le corps.
Cette zone, beaucoup la regardent dans le miroir tous les matins sans imaginer une seconde le rôle qu’elle pourrait jouer.

Table des matières
Le chiffre qui devrait inquiéter tout le monde
D’ici 2030, les Américains de plus de 65 ans représenteront 20 % de la population, soit 71 millions de personnes. Une personne de plus de 65 ans sur neuf est aujourd’hui diagnostiquée Alzheimer aux États-Unis. Et la France n’est pas épargnée par cette dynamique.
Pendant ce temps, un autre indicateur explose. Chez les seniors américains, l’obésité a presque doublé en trente ans, passant de 22 % à 40 % entre 1988 et 2018. Les deux courbes montent en parallèle. Coïncidence ? Les chercheurs n’y croient plus.
Une équipe de Floride réécrit le récit
La revue, signée Shailaja Kesaraju Allani (Florida Atlantic University) et Romina María Uranga (New College of Florida), porte un titre technique : “From Lipids to Mitochondria: Shared Metabolic Alterations in Obesity and Alzheimer’s Disease”. Traduction simple : des lipides aux mitochondries, ce que l’obésité et Alzheimer ont en commun.
Les auteures ont passé en revue les preuves accumulées depuis vingt ans. Leur verdict est sans détour : ces deux maladies, longtemps étudiées séparément, partagent les mêmes pannes biologiques au départ. Pas une, pas deux. Cinq.
Et la plus importante n’a rien à voir avec le cerveau lui-même.
Le tissu graisseux n’est pas qu’un stockage
Première idée à abandonner : la graisse n’est pas un sac inerte. C’est un véritable organe, qui parle au reste du corps en permanence. Il libère des messagers chimiques appelés adipokines (les hormones du tissu adipeux). Certains sont anti-inflammatoires, d’autres pro-inflammatoires. En temps normal, les deux camps s’équilibrent.
Quand le tissu graisseux gonfle de manière excessive, surtout au niveau du ventre, cet équilibre se brise. Le tissu graisseux profond (viscéral, autour des organes) se met à sécréter des signaux d’alarme en continu. Le corps entre dans un état d’inflammation à bas bruit, qui n’éveille aucun symptôme pendant des années.
Cette inflammation finit par franchir une barrière qu’on croyait infranchissable.
La barrière qui n’en est plus une
Le cerveau est protégé du reste de l’organisme par la barrière hémato-encéphalique, une sorte de douane biologique qui filtre ce qui entre. L’inflammation chronique, à la longue, abîme cette douane. Des molécules pro-inflammatoires et même des cellules immunitaires finissent par passer.
Une fois dans le cerveau, ces intrus activent en permanence les cellules de soutien des neurones (microglie et astrocytes). C’est l’entrée dans la neuroinflammation, terrain de jeu favori d’Alzheimer.
Pire encore : les chercheurs ont découvert que le tissu graisseux envoie aussi des micro-paquets, des vésicules extracellulaires, capables de traverser cette barrière. Une étude de 2022, citée dans la revue, a montré que ces vésicules issues de souris obèses, injectées dans des souris saines, provoquaient une perte de connexions entre neurones (synapses) et un déclin cognitif.
Et ce n’est pas le plus inquiétant.
Le suspect numéro un n’est pas celui que l’on croit
Dans la longue liste des coupables potentiels, les auteures en désignent un en particulier. Pas l’inflammation. Pas le sucre. Pas le cholestérol seul.
La défaillance vient d’une structure microscopique présente dans presque toutes les cellules du corps. Une structure que les manuels scolaires appellent “la centrale énergétique de la cellule”.
Le cerveau, lui, est un client gourmand. Il pèse 2 % du poids corporel, mais consomme près de 20 % de l’énergie totale. La moindre coupure de courant met les neurones en péril.
C’est précisément cette panne que l’obésité et Alzheimer ont en commun.
Les mitochondries au cœur du problème
Les mitochondries (prononcer “mi-to-con-drie”) sont de minuscules usines à énergie logées dans chaque cellule. Elles transforment les sucres et les graisses en ATP, la monnaie énergétique du corps. Pour fonctionner, elles utilisent deux chaînes de production : le cycle des acides tricarboxyliques (le cycle de Krebs, vu en cours de SVT) et la chaîne de transport des électrons.
Dans l’obésité comme dans Alzheimer, ces deux chaînes tournent au ralenti. Plusieurs enzymes clés perdent en activité, dont la citrate synthase, l’isocitrate déshydrogénase et l’alpha-cétoglutarate déshydrogénase (les noms n’ont pas besoin d’être retenus, l’idée à retenir est que toute la chaîne grippe en même temps).
Conséquences immédiates :
- Moins d’énergie produite ;
- Plus de molécules instables fabriquées en sous-produits ;
- Une cellule qui s’auto-empoisonne lentement.
Ces molécules instables s’appellent espèces réactives de l’oxygène (ROS). En petite quantité, elles servent de messagers. En excès, elles abîment tout : protéines, lipides, ADN.
C’est ce que les auteures appellent “le stress énergétique”.
Comment ce stress fabrique les plaques d’Alzheimer
À ce stade, le mécanisme se met en place. Quand les mitochondries produisent trop de ROS, la fabrication de la protéine bêta-amyloïde s’emballe. Cette protéine, en s’accumulant, forme les fameuses plaques séniles visibles dans le cerveau des malades d’Alzheimer.
En parallèle, une autre protéine appelée tau se modifie de manière anormale (hyperphosphorylation), formant des enchevêtrements à l’intérieur des neurones. Plaques à l’extérieur, enchevêtrements à l’intérieur : les deux signatures de la maladie sont réunies.
Et le tout démarre dans une cellule qui manque simplement d’énergie.
L’insuline, deuxième pièce du puzzle
Les chercheuses insistent sur un point. Le cerveau possède ses propres récepteurs à l’insuline. Quand le corps devient résistant à l’insuline (cas typique chez les personnes en surpoids ou diabétiques de type 2), le cerveau aussi.
Cette résistance cérébrale à l’insuline a un effet direct : elle perturbe le métabolisme du glucose dans les neurones, ralentit la production d’ATP, et favorise l’accumulation d’amyloïde et de tau. Le phénomène est si net que certains chercheurs surnomment Alzheimer “le diabète de type 3”.
Des études animales ont montré qu’en bloquant la production d’insuline directement dans le cerveau (par injection de streptozotocine), on déclenche en quelques semaines des troubles de mémoire qui ressemblent à Alzheimer. Ces déficits sont partiellement réversibles avec des médicaments antidiabétiques.
Le cerveau et le pancréas parlent la même langue. Quand l’un perd l’oreille, l’autre suit.
Le rôle de l’intestin que personne n’attendait
La revue consacre un chapitre entier à un acteur qui semble très éloigné du cerveau : le microbiote intestinal. Cette population de bactéries, de virus et de champignons logée dans l’intestin pèse environ 1,5 kg et compte autant de cellules que le corps tout entier.
Quand l’alimentation est riche en fibres (régime méditerranéen, légumes, légumineuses), certaines bactéries fabriquent des acides gras à chaîne courte, notamment l’acétate, le propionate et le butyrate. Ces molécules :
- Renforcent la barrière intestinale ;
- Calment l’inflammation ;
- Soutiennent les cellules immunitaires du cerveau ;
- Réduisent les dépôts d’amyloïde dans les modèles animaux.
À l’inverse, une alimentation ultra-transformée et l’obésité font basculer l’équilibre du microbiote (dysbiose). L’intestin devient plus poreux, des fragments bactériens passent dans le sang, alimentent l’inflammation générale, et finissent par nourrir l’inflammation cérébrale.
L’axe intestin-cerveau n’est plus une hypothèse. C’est une autoroute.
Le détail qui change tout : les signes apparaissent avant les symptômes
Voici ce qui rend cette revue particulièrement importante. Les auteures insistent sur un point précis : ces dérèglements métaboliques ne sont pas la conséquence d’Alzheimer. Ils précèdent la maladie. Souvent de longues années.
“Ces changements métaboliques ne surgissent pas une fois la maladie installée, ils commencent bien plus tôt”, explique Shailaja Allani dans le communiqué de presse de Florida Atlantic University. “Ils pourraient même contribuer à déclencher la maladie avant l’apparition des symptômes. Ce sont des signaux d’alerte précoces qui permettraient d’identifier les personnes à risque.”
Autrement dit : un cerveau qui développera Alzheimer à 70 ans envoie probablement des signes mesurables à 50 ans. Pas par les pertes de mémoire, encore inexistantes. Par le métabolisme.
Une nuance importante sur l’âge
Un point étonne au premier abord. L’obésité au milieu de la vie (autour de 50 ans) augmente clairement le risque de démence. Mais chez les personnes très âgées, un poids plus faible est associé à un risque plus élevé de démence et de mortalité. Les chercheurs appellent ce phénomène “le paradoxe de l’obésité”.
L’explication est simple : la perte de poids involontaire chez le sujet âgé reflète souvent un processus pathologique déjà en cours. L’IMC perd alors de sa valeur comme indicateur, parce que la composition du corps change avec l’âge (perte de muscle, redistribution de la graisse).
Le message à retenir : c’est la santé métabolique qui compte, pas le chiffre sur la balance.
Ce que cela change pour la prévention
La revue ne propose pas de traitement miracle. Elle propose un changement de regard. Plutôt que d’attendre les premiers oublis pour agir, surveiller la santé métabolique pourrait identifier le risque très en amont.
Les leviers concrets pointés par la littérature scientifique :
- Améliorer la sensibilité à l’insuline par l’activité physique régulière ;
- Réduire le stress oxydatif par une alimentation riche en antioxydants ;
- Maintenir une masse grasse viscérale basse (le tour de taille reste un meilleur marqueur que le poids) ;
- Préserver un microbiote varié grâce aux fibres et aux aliments fermentés ;
- Limiter l’inflammation chronique par le sommeil, la gestion du stress, l’activité physique.
Aucun de ces points n’est une découverte en soi. Ce qui change, c’est leur enjeu. Ils ne servent plus seulement à éviter le diabète ou l’infarctus. Ils pourraient aussi protéger le cerveau, des années avant qu’il ne donne le moindre signal d’alarme.
La conclusion qui dérange (et qui rassure)
Les auteures terminent leur revue sur une phrase qui résume tout : il faut cesser de traiter l’obésité et Alzheimer comme deux maladies séparées. Ce sont les deux faces d’un même problème métabolique, qui se développe en silence pendant deux décennies avant de se manifester.
Cette information dérange, parce qu’elle rend chacun responsable d’une partie de son destin cognitif. Mais elle rassure aussi : elle ouvre une fenêtre d’action très large. Beaucoup plus large que la fenêtre étroite des traitements actuels, qui agissent une fois la maladie déjà installée.
Le cerveau ne tombe pas malade du jour au lendemain. Il s’épuise. Et il prévient longtemps à l’avance, à condition de savoir où regarder.
Résumé en image
Sur le même sujet
Sources éditoriales et fact-checking