Pendant des années, les cardiologues avaient un angle mort. Une énigme qui tenait tête aux meilleurs spécialistes mondiaux. Des patients arrivaient aux urgences, essoufflés au moindre effort, les chevilles gonflées, le visage marqué par la fatigue. Tous les signes d’une insuffisance cardiaque. Sauf un détail. Un détail qui changeait tout.
Leur cœur, en apparence, pompait normalement.
Sur l’échographie, la fraction d’éjection (c’est-à-dire le pourcentage de sang que le cœur expulse à chaque battement) affichait des valeurs proches de la normale, autour de 65 %. Comme chez vous, comme chez n’importe quelle personne en bonne santé. Et pourtant, ces patients allaient mal. Très mal. Un sur quatre ou cinq meurt dans l’année qui suit le diagnostic.
Alors les médecins ont cherché une explication. Ils ont pointé du doigt la rigidité du muscle cardiaque, son incapacité à se remplir correctement entre deux battements. Le muscle devenait comme une éponge dure qui refuse d’absorber l’eau. Ils ont même donné un nom à cette maladie : l’insuffisance cardiaque à fraction d’éjection préservée, ou HFpEF dans le jargon international.
Sauf que cette explication ne tenait pas la route pour tous les patients.
Et une équipe de Baltimore vient de prouver pourquoi. Leurs résultats, publiés le 23 avril 2026 dans la revue Science(1), remettent en cause ce qu’on pensait savoir depuis vingt ans sur cette maladie. Mieux : ils ouvrent une piste thérapeutique inattendue.

Table des matières
Une énigme médicale qui dure depuis des décennies
Près de la moitié des personnes qui souffrent d’insuffisance cardiaque sont concernées par cette forme particulière. Aux États-Unis, cela représente plusieurs millions de patients. En France, la proportion est similaire. Les médecins les reconnaissent à leurs symptômes : essoufflement, fatigue chronique, jambes qui gonflent, difficulté à monter un escalier.
Historiquement, cette maladie touchait surtout les personnes âgées avec une tension artérielle élevée de longue date, un muscle cardiaque épaissi et souvent un diabète associé. Le profil type : un homme ou une femme de 70 ans et plus, hypertendu depuis longtemps.
Mais depuis une vingtaine d’années, le profil a changé. Silencieusement. Les salles d’attente se sont remplies d’un autre type de patients : des personnes atteintes d’obésité sévère, avec une tension pas forcément si élevée et un cœur pas forcément si épaissi.
Le même diagnostic, mais pas la même maladie ?
C’est l’hypothèse que l’équipe du cardiologue David Kass, à l’école de médecine de l’université Johns Hopkins, a voulu vérifier. Et pour cela, ils n’ont pas choisi la facilité. Ils sont allés chercher directement dans le muscle cardiaque des patients.
Une enquête au microscope sur 80 cœurs malades
Quatre-vingts patients atteints de cette insuffisance cardiaque à fraction d’éjection préservée ont accepté de subir une biopsie (un tout petit prélèvement de muscle cardiaque, fait au cours d’un examen de routine). L’équipe de Kass a ensuite comparé ces échantillons avec du tissu cardiaque provenant de donneurs d’organes sans maladie du cœur, ainsi qu’avec le tissu de personnes en attente d’une greffe de cœur.
Puis les chercheurs ont fait quelque chose d’assez malin. Ils ont confié les données à un algorithme d’intelligence artificielle sans lui donner d’indication. Sa seule mission : regrouper les patients selon les propriétés de leurs cellules cardiaques, sans savoir qui avait quoi.
L’algorithme a tranché. Il a séparé les patients en deux groupes distincts.
Et le critère qui les distinguait n’était pas l’âge. Ni la tension. Ni le diabète. C’était l’indice de masse corporelle (IMC), autrement dit le rapport entre le poids et la taille au carré, l’indicateur utilisé pour classer l’obésité. Un premier groupe avait un IMC moyen de 30 kg/m². Le second, un IMC moyen de 43 kg/m² (ce qu’on appelle une obésité sévère).
Deux IMC différents, deux maladies différentes. Dans le même diagnostic officiel.
Le moment où les scientifiques ont été surpris
Quand les chercheurs ont stimulé les cellules cardiaques du premier groupe (IMC 30) avec du calcium, qui est le signal naturel qui déclenche la contraction du muscle, les cellules ont répondu presque normalement. La force de contraction était à peu près préservée, comme le suggérait la théorie classique.
Mais avec les cellules du second groupe, celui des patients en obésité sévère, la surprise a été brutale.
Ces cellules se sont révélées incapables de produire une contraction puissante. Pire : leurs performances ressemblaient à celles des cellules prélevées sur des patients en attente de greffe cardiaque, des personnes dont le cœur est tellement endommagé qu’il ne peut plus être sauvé autrement.
Autrement dit : des patients considérés comme ayant un cœur qui “pompe normalement” à l’échographie ont, au niveau microscopique, des cellules cardiaques aussi affaiblies que celles de personnes en insuffisance cardiaque terminale.
Le paradoxe tient dans une seule phrase. Et il explique enfin pourquoi ces patients résistent aux traitements classiques.
Pourquoi le muscle cardiaque devient faible
Reste à comprendre le mécanisme. Qu’est-ce qui, dans le muscle, déraille exactement ?
L’équipe s’est alors tournée vers les sarcomères. Ce mot technique désigne les minuscules unités contractiles qui composent chaque cellule musculaire. Imaginez des petits moteurs microscopiques alignés en série, qui se raccourcissent tous en même temps quand le muscle se contracte. C’est eux qui font battre le cœur.
L’analyse par rayons X a révélé que ces moteurs, chez les patients en obésité sévère, présentaient une structure cristalline anormale. Le mécanisme interne était déformé.
Et en creusant encore plus loin, les scientifiques ont trouvé le coupable : une protéine appelée troponine I, essentielle au déclenchement de la contraction. Chez ces patients, cette protéine subissait une modification chimique (une phosphorylation, c’est-à-dire l’ajout d’un groupement phosphate qui change le comportement de la protéine) bien plus prononcée que chez les autres.
En laboratoire, les chercheurs ont démontré que cette seule modification suffit à affaiblir la contraction. La cible moléculaire de la maladie venait d’être identifiée.
Un détail important à noter : chez les personnes en obésité sévère mais sans insuffisance cardiaque, ces anomalies n’étaient pas présentes. L’obésité seule ne détraque donc pas le muscle cardiaque. Il faut la combinaison des deux.
La partie la plus surprenante de l’étude
Et c’est là que l’histoire prend un tournant inattendu.
Un sous-groupe de 16 patients, avec un IMC de départ moyen autour de 39, avait suivi un traitement de perte de poids avant d’être inclus dans l’étude. La plupart d’entre eux avaient reçu un analogue du GLP-1 (la famille de médicaments dont font partie le sémaglutide et le tirzépatide, commercialisés sous les noms d’Ozempic, Wegovy ou Mounjaro). Ce traitement a duré en moyenne un an et demi.
Les chercheurs ont alors analysé leurs cellules cardiaques.
Les cellules avaient récupéré. Pas un peu. Beaucoup.
Les patients qui avaient perdu au moins 10 % de leur poids corporel présentaient une force de contraction cellulaire proche de la normale. Le muscle affaibli redevenait fonctionnel. Le mécanisme cassé se réparait.
David Kass résume ainsi l’idée principale de son travail : l’insuffisance cardiaque à fraction d’éjection préservée, chez les patients en obésité sévère, n’est pas uniquement une histoire de rigidité. C’est aussi une histoire de muscle qui s’affaiblit pour une raison chimique précise. Et cette raison chimique est potentiellement réversible.
Ce que cela change pour les patients
Les implications sont de deux ordres.
Première conséquence, un avertissement. Certains médicaments utilisés dans des maladies cardiaques proches (le mavacamten et l’aficamten, prescrits dans la cardiomyopathie hypertrophique) pourraient être inadaptés voire dangereux chez les patients en obésité sévère atteints de cette forme d’insuffisance cardiaque. Ces molécules agissent en diminuant la force de contraction, or chez ces patients, la force est déjà trop basse. Les chercheurs recommandent donc la prudence.
Deuxième conséquence, un espoir. Deux pistes thérapeutiques émergent :
- La perte de poids encadrée médicalement (y compris par les analogues du GLP-1) pourrait restaurer la fonction cardiaque ;
- Le développement de nouveaux médicaments ciblant directement la modification chimique de la troponine I pourrait permettre de réparer le mécanisme défaillant sans forcément passer par la perte de poids.
Vivek Jani, premier auteur de l’étude et doctorant à Johns Hopkins, le formule avec prudence : il faut soutenir la perte de poids durable et sûre chez ces patients, et parallèlement mettre au point des molécules capables de renverser la modification moléculaire identifiée dans les protéines du sarcomère.
Ce qu’il faut retenir
Pendant vingt ans, on a considéré cette forme d’insuffisance cardiaque comme une maladie de rigidité. Un cœur qui contracte bien mais qui se remplit mal. L’étude de Johns Hopkins montre que, pour une partie des patients (ceux en obésité sévère), cette description est incomplète.
Leur cœur contracte moins bien qu’il n’y paraît. L’échographie ne le voyait pas. Le microscope, si.
Et surtout, cette altération n’est pas une sentence. Chez ceux qui ont perdu suffisamment de poids, le muscle cardiaque s’est rétabli. Un résultat qui replace la gestion du poids, accompagnée médicalement, parmi les leviers thérapeutiques les plus concrets dans cette maladie aux traitements jusqu’ici limités.
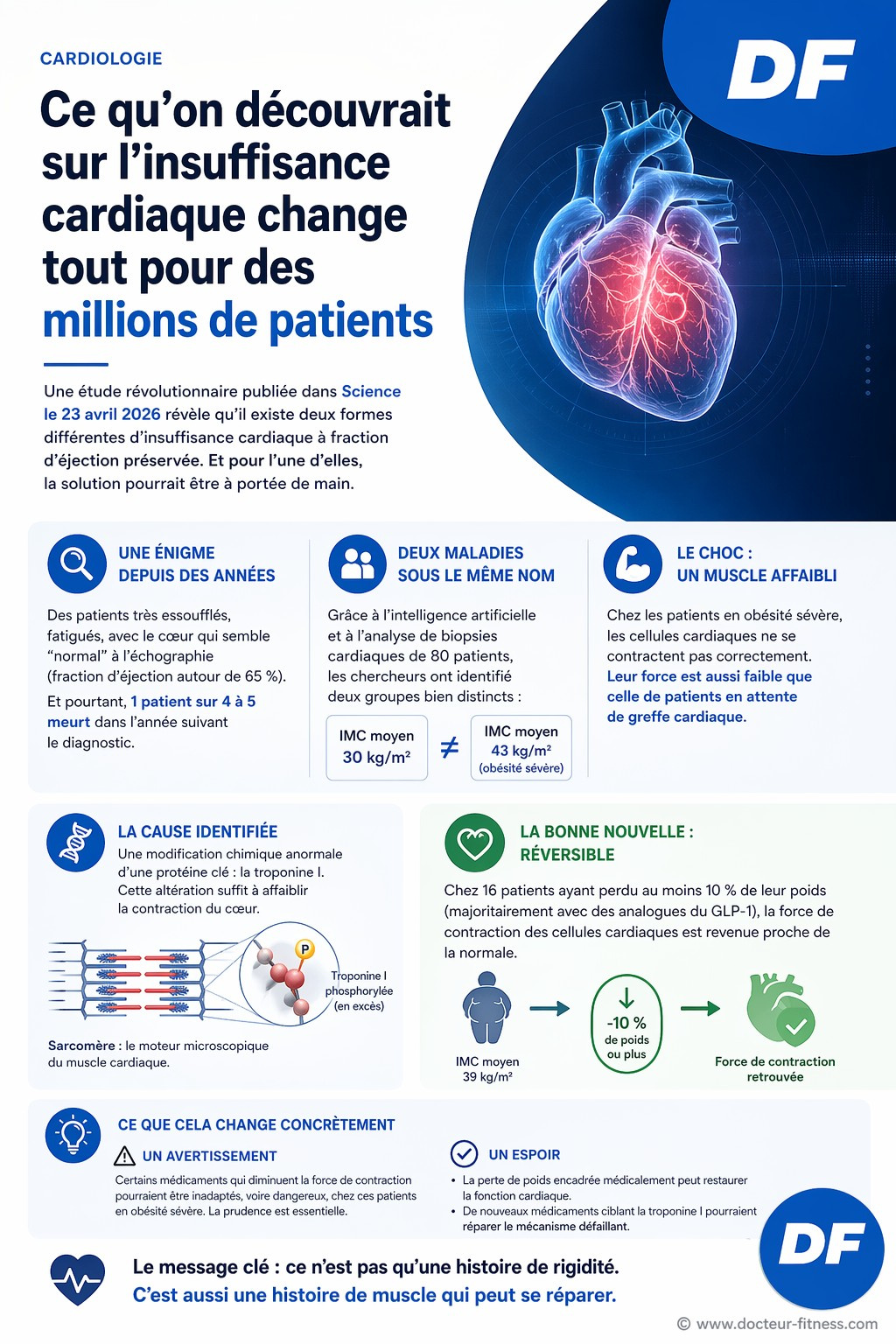
Résumé en image
Sur le même sujet
Sources éditoriales et fact-checking